“In una settimana, da quando è iniziato l’arruolamento dei pazienti per la sperimentazione, abbiamo ricevuto 20 telefonate di persone in cerca di informazioni al numero verde dedicato: ciascuno viene richiamato da un medico del team che sta conducendo lo studio“. La dottoressa Stefania Gori coordina lo studio clinico avviato dal 12 gennaio 2018 all’Ospedale Sacro Cuore Don Calabria di Negrar: lo studio clinico di fase I-II HEPAVAC-101 valuta per la prima volta nell’uomo il vaccino IMA970A, un prodotto innovativo specifico nei confronti dell’epatocarcinoma, il tumore maligno primitivo più frequente del fegato, con una incidenza nel mondo di 750.000 nuovi casi l’anno.
HEPAVAC-101 è uno studio internazionale che si svolge in Germania, Spagna, Francia, Belgio, Gran Bretagna e Italia. Nel nostro Paese vede coinvolti solo due centri: l’Ospedale Sacro Cuore Don Calabria di Negrar – Verona (in collaborazione con l’Università dell’Insubria) e l’Istituto Nazionale Tumori “Pascale” di Napoli

La sperimentazione è riservata ai pazienti con epatocarcinoma in fase iniziale (ad uno stadio molto precoce, precoce ed intermedio), che sono candidati ad un trattamento locale (intervento chirurgico, termoablazione o ablazione mediante radiofrequenza e microonde, chemioembolizzazione, radioembolizzazione). “Cinque di loro sono già stati individuati e ora procederemo con gli esami iniziali per valutare se siano idonei alla sperimentazione”, spiega Gori, che è anche presidente nazionale AIOM (Associazione italiana di oncologia medica), la prima donna in 45 anni di associazione.
La selezione dei pazienti non è conclusa: per informazioni è disponibile il numero 800 143 143 Numero Verde del Cancer Care Center – Ospedale Sacro Cuore Don Calabria (dal lunedì al venerdì dalle ore 9.00 alle ore 12.00)
Gori ribadisce che si tratta di una fase I: “Lo scopo dello studio, al momento, è valutare la tollerabilità del vaccino IMA970A, cioè se determina particolari effetti collaterali, e verificare se il vaccino, somministrato dopo la regressione della malattia ottenuta con il trattamento locale, è in grado di indurre una risposta immunitaria nei confronti del tumore. Se il vaccino IMA970A dimostrasse di indurre una risposta immunitaria, potrebbe ritardare la progressione del tumore o favorire una ulteriore regressione del tumore stesso: questo si valuterà tuttavia in una seconda fase“. Per i primi risultati ci vorrà circa un anno.
Laureata nel 1980, da sempre in questo campo, Gori rimarca che la ricerca “è in oncologia la modalità più importante con cui siamo riusciti e riusciremo a combattere il cancro. Condurre ricerca significa anche migliorare l’assistenza oncologica, così come poter fornire nuovi farmaci, non ancora in commercio e potenzialmente efficaci, a pazienti che necessitano di una alternativa terapeutica. Qui a Negrar, in Oncologia Medica, lavorano insieme oncologi senior e giovani ricercatori: il loro atteggiamento ed entusiasmo e dedizione al lavoro rappresentano una forza incredibile per poter percorrere questi sentieri, difficili, ma che molte volte danno risultati importanti ai nostri pazienti”.
L’intero progetto internazionale che comprende più centri europei è stato finanziato dalla UE con circa 6 milioni di euro.
 La malattia – Oltre il 70% di questi tumori – epatocarcinomi – è riconducibile a fattori di rischio noti e tra questi i più frequenti sono: l’infezione da virus dell’epatite C (HCV), da virus dell’epatite B (HBV), da abuso di bevande alcoliche. In Italia sono stati diagnosticati nel 2017 circa 13.000 nuovi casi. A 5 anni dalla diagnosi la sopravvivenza è del 20%. Al momento le opzioni terapeutiche per questo tumore sono limitate e nel 2014 si sono verificati in Italia oltre 9.900 decessi per tumori del fegato: ecco perché è necessario sviluppare terapie innovative per l’epatocarcinoma al fine di migliorarne la prognosi.
La malattia – Oltre il 70% di questi tumori – epatocarcinomi – è riconducibile a fattori di rischio noti e tra questi i più frequenti sono: l’infezione da virus dell’epatite C (HCV), da virus dell’epatite B (HBV), da abuso di bevande alcoliche. In Italia sono stati diagnosticati nel 2017 circa 13.000 nuovi casi. A 5 anni dalla diagnosi la sopravvivenza è del 20%. Al momento le opzioni terapeutiche per questo tumore sono limitate e nel 2014 si sono verificati in Italia oltre 9.900 decessi per tumori del fegato: ecco perché è necessario sviluppare terapie innovative per l’epatocarcinoma al fine di migliorarne la prognosi.
Attualmente i pazienti con epatocarcinoma in fase iniziale vengono sottoposti a procedure locali che consistono nella resezione chirurgica del tumore laddove possibile, o nella distruzione dei noduli tumorali mediante termoablazione, ablazione con radiofrequenza e microonde, chemioembolizzazione o radioembolizzazione. Nonostante tali trattamenti possano ottenere una distruzione del tessuto vitale del tumore, nel tempo la malattia è destinata a recidivare o a peggiorare nella maggior parte dei casi.
Cos’è IMA970A? – E’ un vaccino a base multipeptidica sviluppato nell’ambito del progetto HEPAVAC, una iniziativa internazionale finanziata dall’Unione Europea che vede la partecipazione di 9 partner europei dei settori farmaceutico ed universitario. I peptidi contenuti nel vaccino sono stati isolati e selezionati a partire dal tessuto tumorale di epatocarcinomi provenienti da centinaia di pazienti. Questi peptidi sono specifici, in quanto presenti soltanto nell’epatocarcinoma e non nei tessuti sani.
Come si svolge lo studio? – I pazienti che prenderanno parte alla sperimentazione verranno sottoposti ad alcuni esami di screening per verificare la loro idoneità a partecipare allo studio, prima di ricevere il trattamento locale standard. I pazienti che, dopo il trattamento locale, non presentano evidenza di tumore vitale riceveranno il trattamento sperimentale. Il trattamento prevede una unica infusione endovenosa di una bassa dose di ciclofosfamide (un farmaco chemioterapico con funzione immuno-modulante).
Dopo pochi giorni viene iniziata la vaccinazione vera e propria. La vaccinazione consiste nella somministrazione intradermica (con ago sottile, a livello della cute del braccio) sia del vaccino IMA970A che di una sostanza adiuvante (che serve cioè a potenziare l’immunogenicità del vaccino e che contiene RNA). Sono previste 9 somministrazioni totali intradermiche del vaccino: le prime 4 vengono effettuate ogni settimana e le altre 5 ogni tre settimane.
Dove si svolge lo studio? – La sperimentazione si svolge presso l’Unità Operativa di Oncologia Medica diretta dalla dott.ssa Stefania Gori in collaborazione con il dott. Alberto Masotto dell’Unità Operativa di Gastroenterologia diretta dal dott. Paolo Bocus.
In molte altre sedi si combatte questa battaglia:
Trento, un’arma di precisione
contro il DNA malato
Era stato salutato da molti come la scoperta biologica più importante del XXI secolo, per la portata globale delle sue applicazioni. Ma le applicazioni del genome editing (cioè la sua correzione) sono state, fin dall’inizio, ostacolate dall’incapacità dell’enzima che riscrive il DNA di essere davvero accurato. Al CIBIO (Centro di biologia integrata) dell’Università di Trento si è trovato il modo di renderlo un’arma di precisione pressoché assoluta, che spara un solo proiettile e uccide il DNA malato.

Questo renderà il genome editing utilizzabile per la correzione delle alterazioni presenti, ad esempio in malattie genetiche e nei tumori. Lo studio trentino è pubblicato dalla rivista “Nature Biotechnology”. Anna Cereseto, autrice senior, dice: «La forza del lavoro è che abbiamo sviluppato una variante della molecola CRISPR/Cas9 più sicura e affidabile di qualunque altra finora descritta, che effettua il taglio di DNA soltanto nel punto voluto». L’obiettivo ora è valorizzare il brevetto derivato dall’invenzione generando ricadute sul territorio trentino.
Il metodo per modificare il DNA a scopo terapeutico, proposto e sviluppato originariamente a Berkley e all’MIT di Boston, è arrivato a Trento per raggiungere l’affidabilità e la sicurezza necessari nelle applicazioni cliniche. E la svolta, integralmente realizzata al CIBIO, potrebbe avere effetti a breve termine per la terapia genica delle malattie.
«Abbiamo messo a punto un metodo sperimentale di screening attraverso il quale otteniamo una molecola, che chiamiamo evoCas9, davvero precisa nel cambiare il DNA. È un enzima di affidabilità assoluta, che effettua il cambiamento soltanto nel punto stabilito» commenta con orgoglio e soddisfazione Anna Cereseto, professoressa del CIBIO e senior author dell’articolo che descrive lo studio su “Nature Biotechnology”, la rivista di biomedicina in assoluto con il maggiore impatto (qui il testo completo disponibile in open access)
«La molecola da cui siamo partiti, CRISPR/Cas9, sta cambiando la faccia della biomedicina. Si tratta di una “macchina molecolare”, fatta della proteina Cas9 e di una molecola di RNA, che raggiunge e taglia uno specifico segmento di DNA, permettendo di modificarne la sequenza. Il problema è che questa molecola fa errori sistematici e quando applicata al tentativo di curare malattie non modifica solo il gene o i geni implicati nella patologia, ma agisce su altri siti del DNA causando effetti imprevedibili. Ciò la rende inaccettabile per la pratica clinica. In questo momento la nostra evoCas9 è la macchina molecolare migliore al mondo per il genome editing» sottolinea Cereseto.
 Il CIBIO sbaraglia così la concorrenza scientifica internazionale. «Il genome editing è davvero la scoperta del secolo in medicina, e non solo» rimarca il direttore del CIBIO Alessandro Quattrone. «Questa scoperta di Anna e dei suoi altrettanto brillanti collaboratori e colleghi è certo a oggi il contributo più importante che abbiamo dato allo sviluppo di terapie. Mesi fa già il gruppo aveva proposto intelligenti miglioramenti al metodo. Si era parlato di “bisturi genomico usa e getta”. Ma con evoCas9 siamo davvero alla differenza fra un utile espediente e un game changer. Grazie a questo studio, che peraltro si integra perfettamente con il precedente, il genome editing può diventare adulto, e il nostro sforzo adesso è far sì che il ritrovato dia frutto, per quanto possibile, in Trentino. L’interesse per questa tecnologia è globale, non è quindi facile trattenerla; stiamo lavorando in molti per partire da casi come questo e fondare il biotech trentino attraendo capitali. È ciò che la nostra Provincia si meriterebbe per aver sempre fortemente creduto nel programma dell’Università che ha generato il CIBIO».
Il CIBIO sbaraglia così la concorrenza scientifica internazionale. «Il genome editing è davvero la scoperta del secolo in medicina, e non solo» rimarca il direttore del CIBIO Alessandro Quattrone. «Questa scoperta di Anna e dei suoi altrettanto brillanti collaboratori e colleghi è certo a oggi il contributo più importante che abbiamo dato allo sviluppo di terapie. Mesi fa già il gruppo aveva proposto intelligenti miglioramenti al metodo. Si era parlato di “bisturi genomico usa e getta”. Ma con evoCas9 siamo davvero alla differenza fra un utile espediente e un game changer. Grazie a questo studio, che peraltro si integra perfettamente con il precedente, il genome editing può diventare adulto, e il nostro sforzo adesso è far sì che il ritrovato dia frutto, per quanto possibile, in Trentino. L’interesse per questa tecnologia è globale, non è quindi facile trattenerla; stiamo lavorando in molti per partire da casi come questo e fondare il biotech trentino attraendo capitali. È ciò che la nostra Provincia si meriterebbe per aver sempre fortemente creduto nel programma dell’Università che ha generato il CIBIO».
Gli ambiti di applicazione del “correttore perfetto” evoCas9 non si limitano alle malattie genetiche e ai tumori, i primi e più ovvii bersagli, ma si estendono agli altri settori non medici in cui il genome editing è ormai essenziale: il miglioramento delle piante di interesse alimentare e degli animali da allevamento.
Come si è arrivati a questa molecola dal rischio di errore vicino allo zero? Spiega Anna Cereseto: «evoCas9 è stata sviluppata sottoponendo Cas9 a una evoluzione darwiniana in provetta, da qui il nome evoCas9. Cas9 nasce nei batteri, dove la sua imprecisione è un vantaggio perché funziona come una sorta di sistema immunitario contro i DNA estranei che, tagliando qua e là, inattiva meglio il nemico. La nostra intuizione è stata di fare evolvere Cas9 in cellule non batteriche, i lieviti, che sebbene semplici sono molto più vicine a quelle umane. Qui l’abbiamo fatta diventare ciò che ci interessa sia: un cesello che intarsia solo dove deve, un’arma di precisione che colpisce in un punto e risparmia tutto il resto. Questo renderà il suo impiego nella clinica finalmente sicuro».
 Lo studio ha generato, accanto alla pubblicazione, un brevetto, già depositato e già oggetto di interessi molteplici.
Lo studio ha generato, accanto alla pubblicazione, un brevetto, già depositato e già oggetto di interessi molteplici.
La ricerca è stata svolta integralmente al CIBIO di UniTrento e ha coinvolto tre unità di ricerca. Il team vede protagonisti il Laboratory of Molecular Virology con Antonio Casini (primo firmatario), Michele Olivieri, Gianluca Petris, Claudia Montagna, Giordano Reginato, Giulia Maule e Anna Cereseto (senior author e responsabile). Poi il Laboratory of Computational Oncology con Francesca Lorenzin, Davide Prandi, Alessandro Romanel e Francesca Demichelis (responsabile). Quindi il Laboratory of Transcriptional Networks con Alberto Inga (responsabile).
Trieste, Colpire il cancro sabotando
la centrale energetica della cellula: il mitocondrio
Il fattore di trascrizione STAT3 è una proteina coinvolta in numerosi processi oncogenici e, come tale, costituisce un interessante ma al contempo difficile bersaglio terapeutico in oncologia. Su Proceedings of the National Academy of Science of the United States of America (PNAS), i ricercatori MOSE dell’Università di Trieste dimostrano come un nuovo, potente inibitore di STAT3 interferisca con l’attività mitocondriale e i processi che regolano le proteine all’interno della cellula tumorale, causandone selettivamente la morte.
Le strategie usate dalle cellule tumorali per garantire la loro sopravvivenza varia molto in dipendenza dal tipo di tumore, dal fatto che si tratti di tumore primario o metastatico, e dalla variabilità genetica delle popolazione delle cellule tumorali. Tuttavia, adattare il metabolismo a diverse condizioni fisiologiche è una delle principali capacità che tutte le cellule tumorali hanno per sopravvivere, proliferare e, soprattutto, resistere alle terapie. Quindi, decodificare i processi alla base della riprogrammazione metabolica del tumore può costituire un’arma estremamente efficace dal punto di vista terapeutico sia nell’identificazione di nuovi bersagli molecolari che nella progettazione e lo sviluppo di nuovi percorsi curativi.
I mitocondri sono degli organelli cellulari in grado di svolgere molteplici funzioni tra cui la principale è quella di essere la vera e propria centrale energetica e di riprogrammazione metabolica della cellula. Inoltre, studi molto recenti hanno proposto che i mitocondri giochino un ruolo fondamentale nell’adattamento metabolico e nella resistenza ai farmaci propri delle cellule tumorali. La proteina STAT3 (Signal Transducer and Activator of Transcription 3), in aggiunta al suo ruolo canonico di controllore della velocità di trascrizione delle informazioni genetiche dal DNA all’RNA messaggero, è un fondamentale agente regolatore delle funzioni mitocondriali. Quindi, la possibilità di bloccare le attività di STAT3 attraverso un inibitore selettivo che interferisca in maniera negativa con i meccanismi di sopravvivenza e proliferazione delle cellule tumorali può costituire una efficace ed alternativa strategia terapeutica in campo oncologico.
In questo innovativo settore di ricerca, di natura necessariamente multidisciplinare, due ricercatori MOSE dell’Università degli Studi di Trieste, Sabrina Pricl ed Erik Laurini, hanno pubblicato sulla prestigiosa rivista Proceedings of the National Academy of Science of the United States of America (PNAS) i risultati di uno studio internazionale che parte dal computer per arrivare fino in vivo. Tale studio è stato condotto assieme ai colleghi svizzeri (Istituto Oncologico della Svizzera Italiana) e statunitensi (New York University School of Medicine). L’articolo ha avuto come editore il Prof. James E. Darnell, insigne scienziato americano nel campo della biologia cellulare ed autore del testo “Molecular cell biology” adottato in tutti i paesi del mondo come libro riferimento nel settore.
In tale studio, si dimostra per la prima volta come il nuovo farmaco OPB-5602 – prodotto dalla Otsuka Pharmaceuticals (azienda Giapponese che ha contribuito anche al supporto finanziario della ricerca di tutti gli scienziati coinvolti) ed ora già in fase clinica – sia in grado di legarsi con grande affinità a STAT3. L’inibizione dell’attività della proteina provoca a sua volta una complessa serie di eventi a cascata che culminano con un malfunzionamento dei mitocondri e la susseguente morte delle cellule tumorali. Oltre che in vitro, i risultati sono stati riprodotti in vivo, confermando così l’ipotesi alla base dello studio che colpire una cellula tumorale al suo cuore energetico e di riprogrammazione metabolica può costituire un nuovo razionale per lo sviluppo di nuove ed efficaci terapie in campo oncologico.
“I risultati ottenuti nel nostro studio ̶ dichiara il dr. Erik Laurini, primo autore di questo lavoro assieme ai colleghi svizzeri Davide Genini e Lara Brambilla ̶ dimostrano per la prima volta ed in maniera inequivocabile come l’inibizione di STAT3 da parte di OPB-5602 porti a una disfunzione mitocondriale che ha, come conseguenza ultima, un’azione selettiva letale sulle cellule tumorali che basano la loro capacità di sopravvivenza e proliferazione proprio sul funzionamento ottimale della loro centrale energetica e sulla riprogrammazione metabolica a livello mitocondriale.”
“Come ho già avuto modo di affermare in altre occasioni come questa”, aggiunge la Prof.ssa Pricl, “solamente la costituzione di un gruppo di ricerca veramente multidisciplinare, in cui gli scienziati integrano le loro conoscenze di chimica, biofisica, medicina, biologia molecolare, biologia strutturale e computazionale, può portare al traguardo dell’implementazione efficace della ricerca traslazionale attraverso l’identificazione di nuovi approcci terapeutici efficienti. Il nostro gruppo, grazie anche a numerosi finanziamenti nel settore, primo tra tutti quello di AIRC, ci ha permesso di espandere notevolmente la nostra attività in campo sperimentale, spingendo così l’integrazione delle tecniche in silico/in vitro nei campi della biofisica, della biologia strutturale e di quella molecolare ai suoi massimi livelli.”
PreCanMed:dal Friuli Venezia Giulia al Tirolo
la ricerca sul cancro non ha frontiere
Il 25 e 26 gennaio 2018 l’Università degli Studi di Udine ha ospitato i partner austriaci, la Medizinische Universität Innsbruck e l’Austrian Drug Screeening Institute, e quelli italiani, il Consorzio Interuniversitario per le Biotecnologie – Laboratorio Nazionale (LNCIB), quale coordinatore del progetto, e l’Università degli Studi di Trieste, per presentare alla comunità scientifica e ai cittadini, i progressi più recenti conseguiti nel campo della medicina anticancro di precisione.
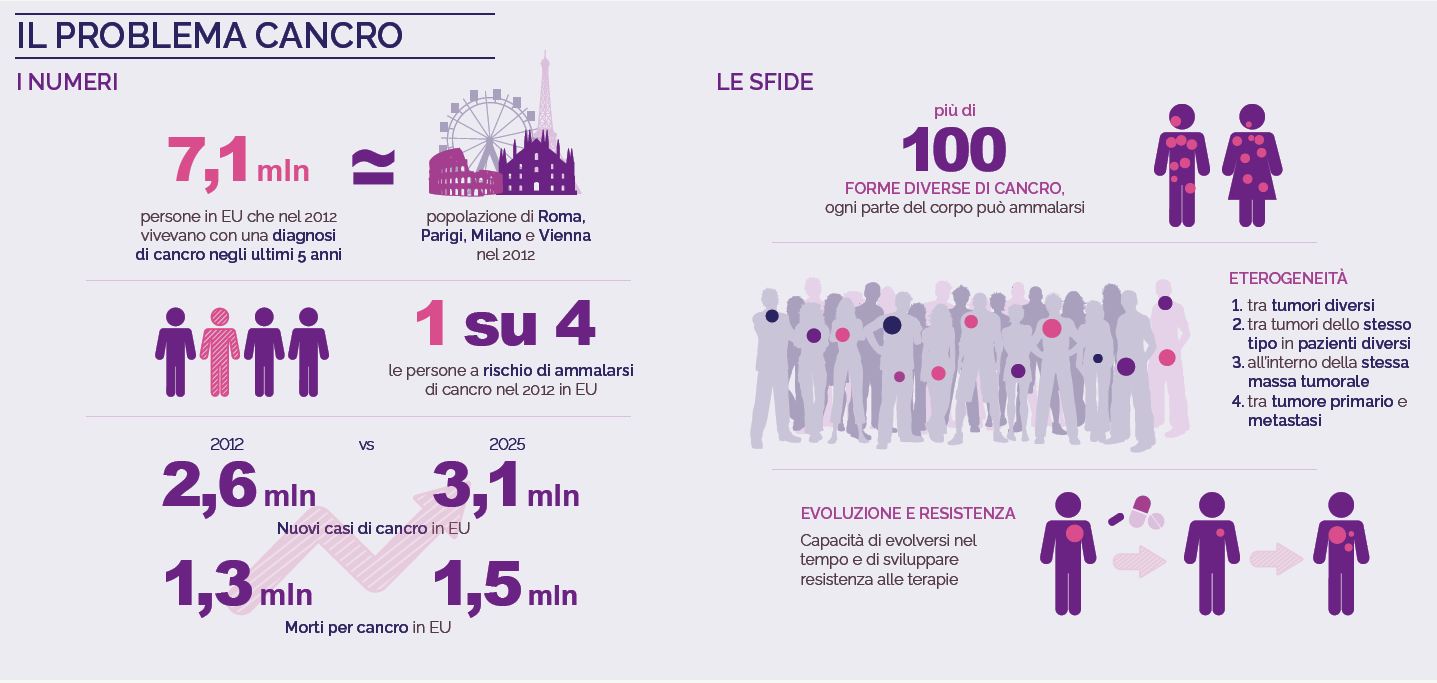 Il progetto trans-frontaliero PreCanMed, partito nel Gennaio 2017 e che durerà tre anni, è finanziato dall’Unione Europea, dal Fondo europeo di sviluppo regionale e dall’Interreg V-A Italia-Austria 2014-2020. Il suo obiettivo è incrementare le potenzialità del Friuli Venezia Giulia e del Tirolo nel settore ricerca e innovazione, costruendo così le premesse per una leadership transfrontaliera nell’ambito della ricerca sul cancro. Sito internet: www.precanmed.eu.
Il progetto trans-frontaliero PreCanMed, partito nel Gennaio 2017 e che durerà tre anni, è finanziato dall’Unione Europea, dal Fondo europeo di sviluppo regionale e dall’Interreg V-A Italia-Austria 2014-2020. Il suo obiettivo è incrementare le potenzialità del Friuli Venezia Giulia e del Tirolo nel settore ricerca e innovazione, costruendo così le premesse per una leadership transfrontaliera nell’ambito della ricerca sul cancro. Sito internet: www.precanmed.eu.
PreCanMed prende in esame un aspetto cruciale del processo di realizzazione della medicina anticancro di precisione, ossia lo sviluppo di nuovi modelli che fedelmente rappresentino le caratteristiche della malattia di un paziente.
In quest’ottica, saranno sviluppati organoidi derivati da cellule tumorali di ciascun paziente, sfruttando una tecnologia innovativa che permette a tali cellule di crescere in laboratorio, su una piastra di coltura. La disponibilità di questo tipo di modello consentirà da un lato di accelerare la sperimentazione di farmaci e di sviluppare in modo più meticoloso e rapido gli interventi di medicina di precisione, che costituiscono il futuro della cura dei tumori, dall’altro permetterà di indirizzare la ricerca verso una più precisa caratterizzazione molecolare del tumore e del paziente.
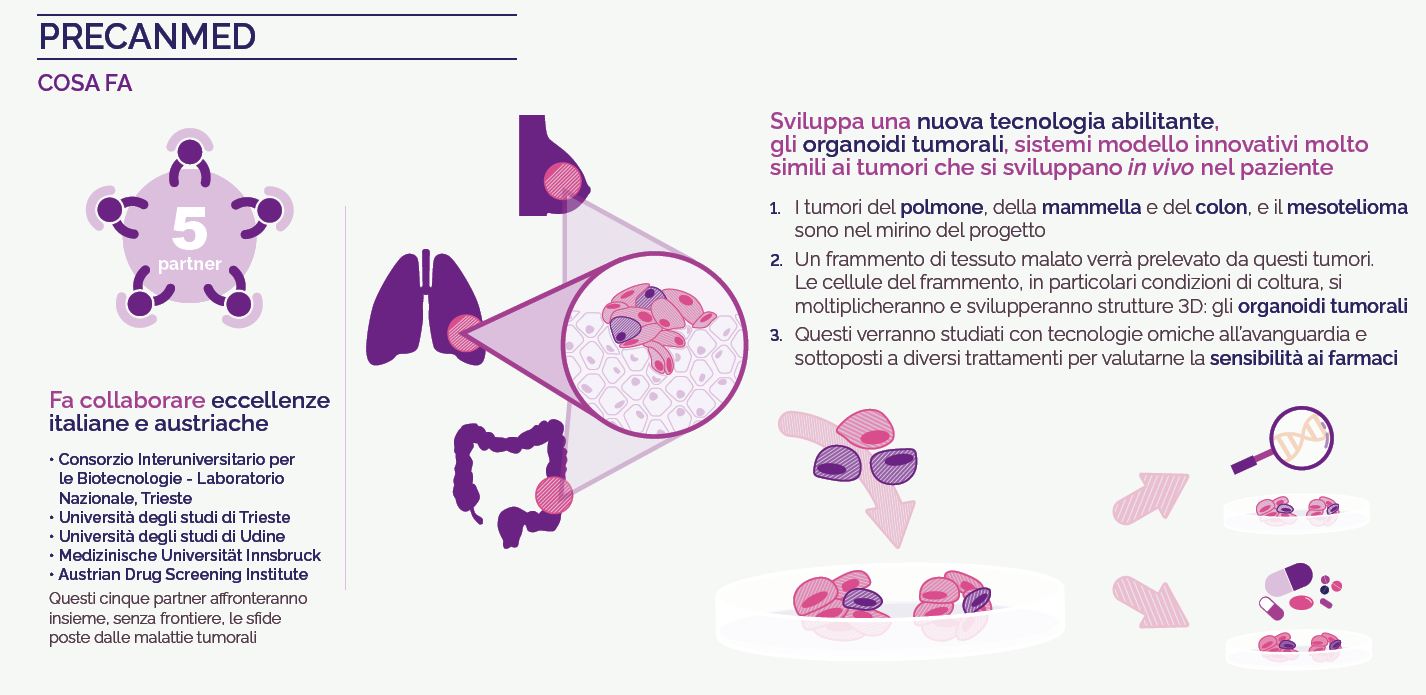 La ricerca svolta dal team di PreCanMed si focalizza in particolar modo sull’ottenimento di organoidi dei tumori della mammella, del colon, del polmone e del mesotelioma, con l’obiettivo di creare la prima Biobanca trans-frontaliera italo-austriaca di organoidi tumorali, che conserverà i modelli sviluppati e tutti i dati molecolari generati. L’intento è rendere accessibile la Biobanca alla comunità scientifica a livello regionale, nazionale e internazionale attraverso accordi di collaborazione con PreCanMed.
La ricerca svolta dal team di PreCanMed si focalizza in particolar modo sull’ottenimento di organoidi dei tumori della mammella, del colon, del polmone e del mesotelioma, con l’obiettivo di creare la prima Biobanca trans-frontaliera italo-austriaca di organoidi tumorali, che conserverà i modelli sviluppati e tutti i dati molecolari generati. L’intento è rendere accessibile la Biobanca alla comunità scientifica a livello regionale, nazionale e internazionale attraverso accordi di collaborazione con PreCanMed.
Il 25 gennaio 2018 i partner PreCanMed si sono riuniti nell’Ateneo udinese, in un evento organizzato dal Prof. Gianluca Tell del Dipartimento di Area Medica come partner del progetto, per condividere con ricercatori, medici, studenti, giornalisti e cittadini i risultati ottenuti dall’avvio del progetto di cooperazione.



